简介
阿尔茨海默病(Alzheimer's disease,AD)是一种多发于老年群体的
神经退行性疾病,最初由德国医生Alois ALZHEIMER 于1907年发现并命名[1]。据统计,全球约有>5000万AD患者,预计到21世纪中期将增加到≥1.52 亿,全球医疗总费用达到8180亿美元,对医疗体系、社会经济造成沉重负担[2]。
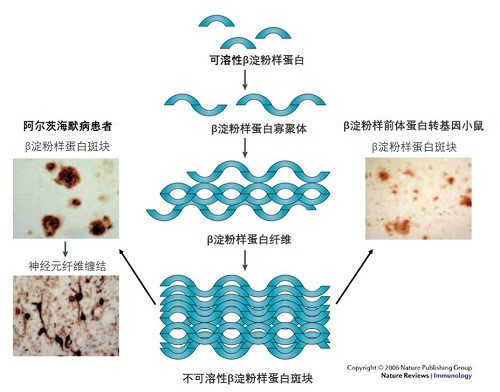
AD是一种非常复杂的神经退行性疾病,病理学机制至今尚未明确,现有几种主流的假说。胆碱能假说认为大脑基底层胆碱能神经元的退化和大脑皮层胆碱能神经传递功能的丧失,导致了AD病人认知功能的衰退[3],目前美国FDA批准的三种胆碱酯酶抑制剂(多奈哌齐、加兰他敏、卡巴拉汀)用于治疗AD就是基于此种假说。淀粉样蛋白级联假说认为AD的发病是由于大脑内异常的Aβ淀粉样蛋白产生和聚集,形成不可溶性的具有神经毒性作用的寡聚物所致[4]。另一种假说认为AD的发病是由于大脑皮层下和内侧颞边缘区中磷酸化的tau蛋白(p-tau)功能失调所致,Aβ蛋白(β-amyloid,Aβ)的聚集加速了p-tau蛋白相关的神经变性的广泛扩散[5]。
AD的临床研究
在AD临床研究中,常见的生物标志物一般可归纳为以下三类[6-7]:
(1)通过核磁共振成像(MRI)测定的
海马体积;
(2)脑脊液生物标志物:
t-tau蛋白、p-tau蛋白和Aβ淀粉样蛋白(40个或42个氨基酸组成的Aβ蛋白,即Aβ40,Aβ42);
(3)正电子放射断层造影术(PET)测定的大脑中的
Aβ淀粉样蛋白图像。
AD主要临床表现为早期记忆力逐渐下降、轻微认知损伤,中后期记忆力明显下降,并出现语言和运动障碍及人格改变等。AD主要标志性病理学特征包括神经元胞外β淀粉样蛋白聚集成老年斑(senile plaques,SP)、tau蛋白异常磷酸化形成神经原纤维缠结(neurofibrillary tangles,NFT)和神经元丢失等。由此,根据其病理特征提出相关发病机制的假说,包括氧化应激(oxidative stress,OS)损伤、tau蛋白异常磷酸化、胆碱能损伤、铝中毒和Aβ毒性等,并在相关假说的基础上建立AD 动物模型。
阿尔茨海默症研究模型
第一类以衰老为基础的老化模型,年龄是AD发病的重要危险因素之一。动物模型以高龄老化作为AD的发病基础,可自发形成。一方面符合衰老或老化生理特征,另一方面无需人为干预,减少了人为因素参与所产生的误差,主要包括自然衰老模型和快速衰老模型,另外还有D半乳糖(D-gal)诱导的亚急性衰老模型、臭氧损伤衰老模型、去胸腺衰老等模型。
第二类各种因素诱发的模型,以AD疾病发生病理假说为基础,采用各种干预手段对实验动物进行干预,来制备相应动物模型。通过手段的不同又分为物理损伤,化学损伤,以及饮食诱导产生的模型。比如颈动脉结扎模型为代表的物理损伤,Aβ注射和鹅膏蕈氨酸注射模型为代表的化学损伤和高脂食物诱发的食物诱导模型。
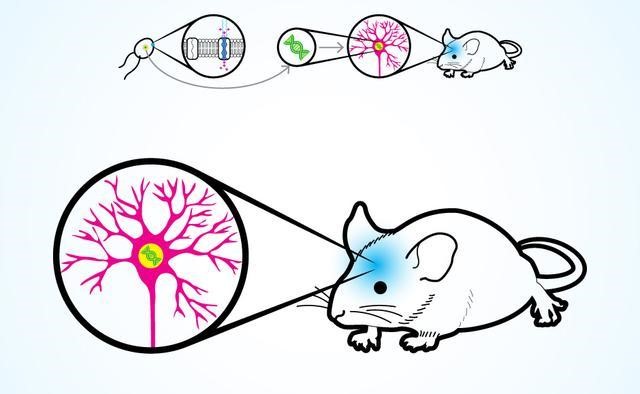
第三类是以遗传学说为其基础,将人或动物的疾病相关基因作为目的基因进行修饰,再拼接一个特定的启动子后植入动物(最常用为小鼠,少数为大鼠、果蝇、斑马鱼)受精卵内。再将受精卵导入假孕动物体内使其稳定遗传以复制AD特定病理特征的各种转基因模型:比较常见的有APP,PS-1,PS-2及apoE4等单转基因模型。另外也有在单转基因模型的基础上结合其他种单转基因模型构建而成的双/多转基因模型。例如,APP/PS双转基因小鼠通过加速表达Aβ,实现更快速且稳定地形成Aβ增多、聚集的病理特征表现。但这类模型与APP模型一样,无法形成Tau病理。而APP/Tau双转基因小鼠可同时出现Aβ斑块沉积和神经元纤维缠结。
目前常用的AD实验动物模型众多,表现出的疾病症状及病理改变各不相同,各种动物模型都有各自的长处与不足,因此需要根据疾病发生原理和实验目的不同选择相应的模型。
一站式服务
布林凯斯在神经系统疾病相关药效药理评价领域,能为您提供一站式从基因分子层次到细胞组织层次,再到神经环路,最后到动物作为整体的行为学评价平台。
在基因分子层次,通过
基因编辑,基因干扰,原位杂交,免疫组化等技术手段,验证基因或蛋白对于细胞生理代谢信号转导、基因表达调控等影响进行研究,并在此基础上结合行为实验验证某分子的功能。
在神经环路层次,我们可以通过
环路示踪、光遗传学、化学遗传学、电生理等手段分析不同脑区、不同类型神经元之间形成的神经环路结构和功能。此类研究是目前神经科学的重点发展方向之一。理解神经元联系变化带来的巨大表型差异,并对其进行深入的操作和分析。
同时,布林凯斯也提供神经系统疾病造模后的
高精度动物行为检测平台包括但不限于:认知功能检测,运动功能检测,清醒动物多通道在体电生理记录、呼吸记录、听觉、痛觉、焦虑、抑郁、嗅觉功能相关的行为学检测等。
还可提供
MRI/fMRI/PET-CT的小动物活体成像,心脏超声,X光片,组织荧光成像(全脑玻片扫描、组织免疫荧光成像)、钙成像、共聚焦双光子成像。
布林凯斯提供全流程定制化实验,包括方案设计,模型制备,数据采集,分析处理,药效评价一站式平台,欢迎垂询。
[1] ALZHEIMER A,STELZMANN RA,SCHNITZLEIN HN,MURTAGH FR. An English translation of Alzheimer′s 1907 paper,“Uber eine eigenartige Erkankung der Hirnrinde”[J]. Clin Anat,1995,8(6):429-431.
[2] FLEMING R, ZEISEL J, BENNETT K. World Alzheimer Report 2020:design dignity dementia:dementia- related design and the built environment Volume 1[R/OL]. London,England:Alzheimer′s Disease International,2020[2020-09-16]. https://www.alzint.org/about/dementia-facts-figures/.
[3] Hampel H, Mesulam MM, Cuello AC, et al. The cholinergic system in the pathophysiology and treatment of Alzheimer's disease [ J]. Bra in, 2018, 141(7): 1917-1933.
[4] Hardy J, Selkoe DJ. The amyloid hypothesis of Alzheimer's disease: progress and problems on the road to therapeutics J] . Science, 2002, 297(5580): 353356.
[5] Ballatore C, Lee VM, Trojanowski JQ. Tau-mediated neurodegeneration in Alzheimer's disease and related disorders [J]. Nat Rev Neurosci, 2007, 8(9): 663672.
[6] Cummings J, Lee G, Ritter A, et al. Alzheimer's disease drug development pipeline: 2019 J. Alzheim- ers Dement (NY), 2019, 5(2): 72-93.
[7] Cummings J, Lee G, Ritter A, et al. Alzheimer's disease drug development pipeline: 2020 J. Alzheim- ers Dement (NY), 2020, 6(1): e12050.