大脑神经网络是由数目庞大,以及形态、特性各异的神经元,通过突触连接构成的复杂结构,是大脑行使认知、情感、记忆、想象等活动的结构基础。绘制神经元投射图能够追踪不同脑区之间的信息流动。
顺向追踪常用方法
一、顺行示踪剂
顺行示踪剂主要被神经元胞体和树突吸收,然后运动至轴突,从而标记该神经元投射的区域。经典的顺行示踪剂主要包括以下几种类型:
1.植物血凝素(PHA-L),具有所显示的神经纤维末梢形态非常细致的优点,基本上没有过路纤维标记问题。
2.放射性标记的氨基酸,这些氨基酸被吸收并掺入到神经元的蛋白质中,通过运动至轴突,也能够从轴突末端释放,并被对应的突触后神经元吸收。
顺向追踪通常与原位杂交、免疫染色或尼氏染色法一起使用。
二、顺行示踪病毒
经典顺行示踪剂的局限在于,注射位点的所有细胞都会吸收示踪剂,因此这种方法所显示的投射模式是不同类型神经元投射的整体反映。而病毒作为神经元追踪试剂,既能在方向上做到更严谨,并能结合Cre-LoxP技术实现细胞类型特异性标记,还具备携带基因工具(如光遗传工具、钙敏感染料、基因编辑工具、RNA干扰工具等)的能力,可在神经环路功能的研究中发挥重要作用。
常用的一些不跨突触的辅助病毒载体包括血清型为2型,8型,9型的腺相关病毒、逆转录病毒和用VSV-G包装的慢病毒等。
三、案例展示
实例一POMC神经元全脑传出的鉴定
实验动物:POMC-Cre小鼠
使用的病毒:AAV9-DIO-mtdTomato,AAV9-DIO-EmGFP
注射部位及病毒量:ARC和NTS,体积各300nl,滴度2.00E+12vg/mL
检测方法:为较好的标记轴突,一个月后灌流取材,荧光纤维镜成像
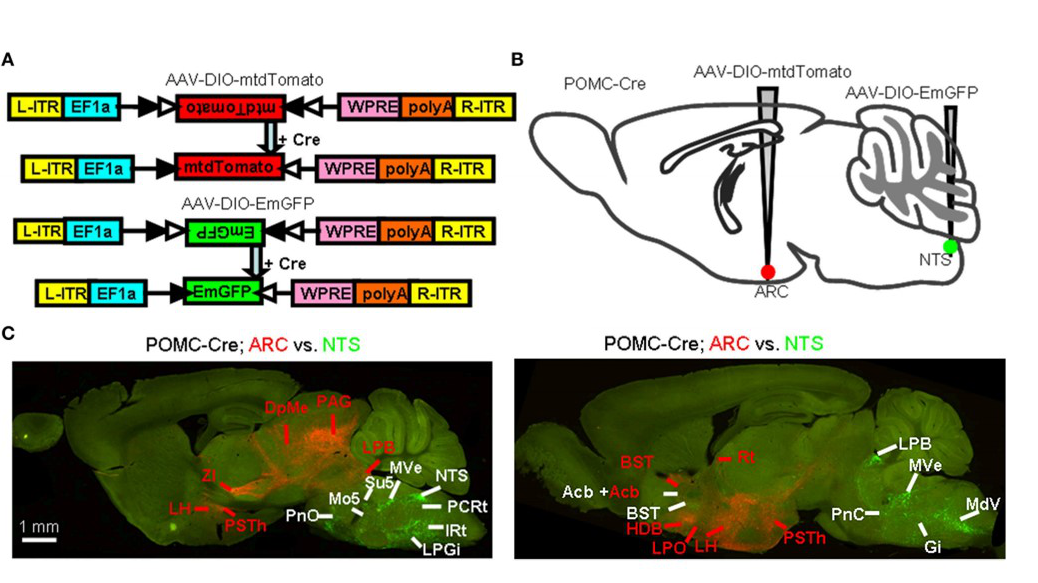 图1. POMC神经元全脑传出的鉴定(Minmin Luo,et al.Frontiersin Neuroanatomy.2015)
图1. POMC神经元全脑传出的鉴定(Minmin Luo,et al.Frontiersin Neuroanatomy.2015)
实例二Dyrk1a(双特异性酪氨酸-(Y)-磷酸化调节激酶1A)在脑发育中的作用
实验动物:出生前和出生后的小鼠
使用的质粒:慢病毒质粒
实验方法:宫内电穿孔注入E14.5小鼠脑室,P0处死小鼠,取材,成像。
 图2. Dyrk1a(WT)过表达可延迟小鼠胚胎皮质发育中神经元的迁移(ZLQiu, et al.MolecularPsychiatry.2018)
图2. Dyrk1a(WT)过表达可延迟小鼠胚胎皮质发育中神经元的迁移(ZLQiu, et al.MolecularPsychiatry.2018)
逆向追踪常用方法
一、逆行示踪剂
逆行示踪剂通常被轴突末端吸收然后反向运输到胞体。经典的逆行示踪剂包括:
1.辣根过氧化物酶(HRP):用于追踪周围神经及中枢神经系统的纤维联系。
2.霍乱毒素亚基b(CTb):是一种很灵敏的顺、逆向追踪剂。CTb是其中一个亚单位,为与细胞受体结合单位,无毒性,其作追踪剂效果更佳。
确定一个示踪剂究竟是正向还是逆向运输主要靠观察。逆行示踪剂通常与选择性富集在轴突末端的受体结合,通过轴突末端的内吞作用被吸收,通过内源的逆向轴突运输系统到达胞体。
二、逆行示踪病毒
和经典的顺行示踪剂一样,上述传统的逆行示踪剂也具有方向不特异,不能实现同一靶区域内特异类型神经元的追踪。
常用的一些不跨突触的逆行病毒载体有:
1.血清型为Retro的腺相关病毒AAV,具有逆行标记效率高、应用广泛、临床应用潜力大等优点。
2.缺失RV-G基因的重组狂犬病毒,携带GFP、mCherry等荧光蛋白基因,可使外源蛋白在神经元中高丰度表达,从而清晰地标记神经元的精细形态。
3.犬腺病毒2型(CAV-2),具有低免疫毒性以及对神经元的偏好性感染的优点。CAV-2病毒还是辅助病毒依赖的病毒粒子,拥有大约30kb的克隆装载量,这些基本性质扩展了CAV-2在中枢神经系统基因治疗中的作用。
三、案例展示
实例一LC-SC投射的逆行病毒示踪
实验动物:WT小鼠
检测方法:AAV-Retro-Cre注射在SC,AAV9-DIO-mCherry注射在LC,4周后可以在LC检测到mCherry荧光信号。
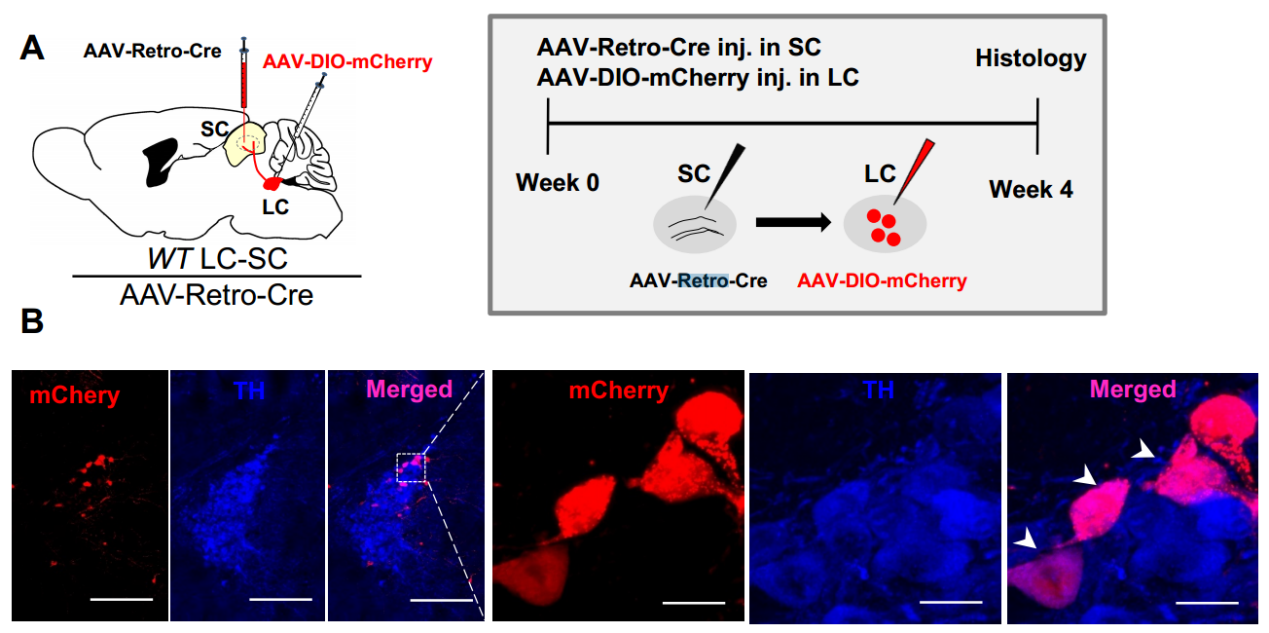 图3. LC-SC投射的逆行病毒示踪(LipingWang, et al.Current Biology.2018)
图3. LC-SC投射的逆行病毒示踪(LipingWang, et al.Current Biology.2018)
实例二VTA能神经元分离的支配NAC和mOT
实验动物:C57BL/6mice
使用的病毒:RV-DG-DsRed和RV-DG-GFP,滴度10的8次方TU
实验方法和结果:分别注入100nlRV-DG-DsRed和RV-DG-GFP在NAC和mOT中,1周后灌流取材,可在VTA追踪到神经元。
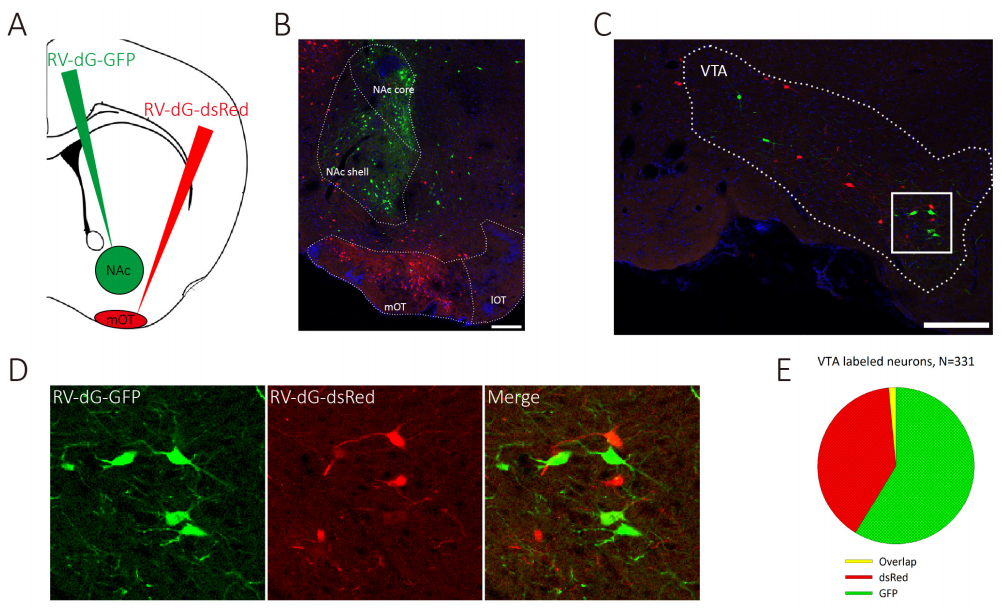 图4. TA能神经元分离的支配NAC和mOT(Zhijian Zhang, et al.eLife.2017)
图4. TA能神经元分离的支配NAC和mOT(Zhijian Zhang, et al.eLife.2017)




